Quem dá mais?
O que se sabe sobre as candidatas a vacina anunciadas pelo Butantan e por Marcos Pontes
Publicado 29/03/2021 às 08:28
Essa nota faz parte da nossa newsletter do dia 29 de março. Leia a edição inteira. Para receber a news toda manhã em seu e-mail, de graça, clique aqui.
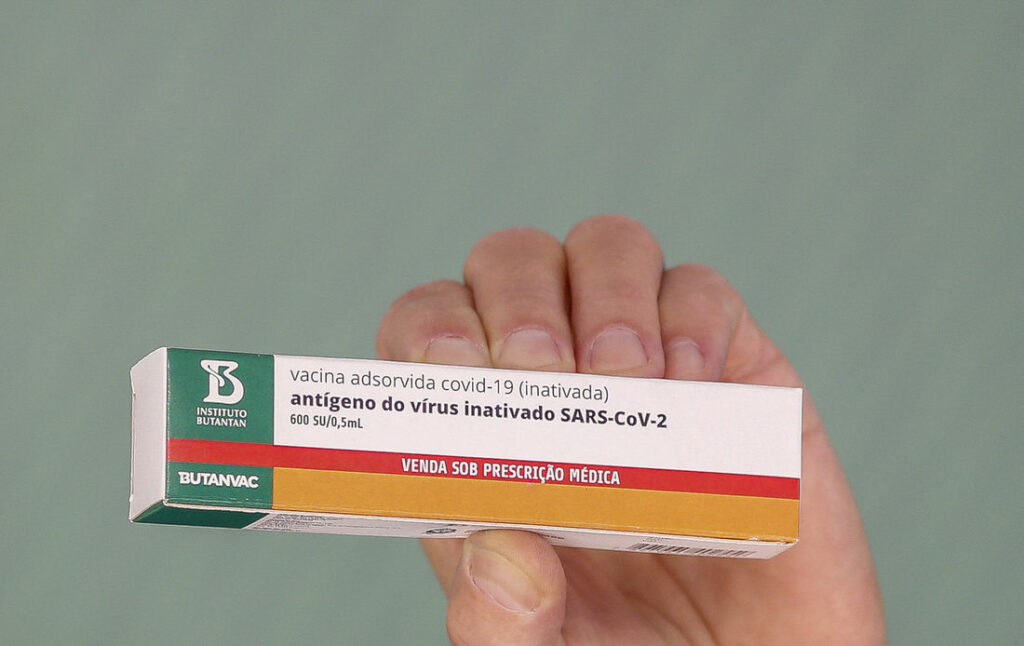
Na sexta de manhã, o Instituto Butantan anunciou o desenvolvimento de uma nova vacina contra a covid-19, a ButanVac, dizendo que no mesmo dia pediria à Anvisa para iniciar os testes clínicos. Horas depois, o ministro da Ciência e Tecnologia Marcos Pontes tentou chegar junto: disse que outros imunizantes nacionais também estão em estágio avançado de pesquisa, e que um deles, desenvolvido pela Faculdade de Medicina de Ribeirão Preto (FMRP), já havia pedido autorização da agência reguladora para o início dos testes em humanos.
Vamos por partes. Não sabemos muita coisa sobre a ButanVac além de que sua tecnologia usa um vetor viral da Doença de Newcastle, uma infecção respiratória que afeta aves, mas não humanos. Esse vetor leva a proteína Spike do coronavírus para o organismo, estimulando a produção de anticorpos. O pedido do Butantan é para a Anvisa liberar o começo das fases 1 e 2, mas o instituto não forneceu nenhum dado sobre os resultados dos testes em laboratório.
O diretor Dimas Covas disse em coletiva de imprensa que o imunizante poderia ser produzido em larga escala a partir de maio, com a população recebendo as doses a partir de julho. Até o fim do ano, haveria 40 milhões de doses disponíveis. “É um momento de profunda esperança para todos nós. Dia 26 de março é o dia da esperança”, disse o animado governador de São Paulo, João Doria (PSDB).
A esperança é real, até pela excelência do Butantan. Mas mas o cronograma anunciado, nem tanto. Mesmo que a autorização da Anvisa para os testes chegue logo e eles comecem em abril, é praticamente impossível terminar todas as etapas até julho, dizem especialistas ouvidos pela BBC. Só as fases 1 e 2 levam de dois a três meses, já em um cenário de abreviação. A fase 3, com dezenas de milhares de participantes, levaria ainda mais alguns meses. E, claro, em qualquer etapa há o risco de o produto não cumprir o que promete e ficar pelo caminho. Para comparação: a Pfizer começou seus ensaios clínicos em maio do ano passado e entregou seus resultados preliminares seis meses depois, em novembro. E isso foi considerado muito rápido.
Outro problema da divulgação pelo governo de São Paulo é a informação de que essa vacina seria “100% nacional, integralmente desenvolvida e produzida no Brasil pelo Instituto Butantan”, como disse João Doria. Não é bem assim. Como mostra a Folha, a tecnologia foi desenvolvida nos Estados Unidos, por pesquisadores do Instituto Mount Sinai. O Butantan afirmou depois que fez uma parceria e tem licença de uso e exploração de parte dessa tecnologia, portanto ela é livre do pagamento de royalties. Além disso, a produção vai ser integralmente nacional, inclusive a do Ingrediente Farmacêutico Ativo (IFA). E isso, considerando o sufoco que se corre a cada atraso na entrega de matéria-prima, é uma grande coisa.
Quanto à vacina anunciada por Marcos Pontes, não é a primeira vez que ouvimos falar dela. Em janeiro, ele mencionou não apenas este produto como outros dois que estariam “a ponto de bala”, prontos para começar os testes em humanos. Mas na época faltava uma coisinha: dinheiro. No caso do imunizante desenvolvido pela FMRP, o problema parece ter sido contornado. Pontes disse que os documentos foram entregues à Anvisa na véspera do pedido do Butantan, para realizar as fases 1 e 2 com 360 pessoas. O fato de o anúncio ter vindo logo após o de João Doria foi, nas palavras do ministro da Saúde Marcelo Queiroga, apenas uma “coincidência“.
Se essa corrida servir para tirar mais candidatas do papel e da fase pré-clínica, está ótimo. Até agora, há 16 projetos de pesquisa sobre candidatas a vacina no país, com testes em células ou em animais. Várias instituições estão envolvidas, entre elas, a Fiocruz, a USP, a UFPR e a UFRJ.
Só não dá para perder de vista que, com a pandemia matando mais do que nunca no país, a prioridade máxima precisa ser conseguir obter e distribuir as vacinas que já foram aprovadas.
Essa nota faz parte da nossa newsletter do dia 29 de março. Leia a edição inteira. Para receber a news toda manhã em seu e-mail, de graça, clique aqui.
Outras Palavras é feito por muitas mãos. Se você valoriza nossa produção, seja nosso apoiador e fortaleça o jornalismo crítico: apoia.se/outraspalavras
